Punto de partida de KAT

Hay varias generaciones de terapias que coexisten como agentes anticancerígenos.
Pero aún la conquista del cáncer está lejos.El mayor problema del tratamiento contra el cáncer que se presenta actualmente es la toxicidad.
En otras palabras, porque no hay selectividad para las células cancerosas.Estamos desarrollando un agente contra el cáncer que se conoce como la cuarta generación de agentes contra el cáncer.
KAT se refiere a la tecnología de tratamiento contra el cáncer desarrollada por el Dr. Ko KAT = Kodiscovery Anticancer TechnologyEsta técnica proviene de una pequeña molécula llamada 3-bromopiruvato (3BP) descubierta por el Dr. Young Hee Ko cuando el Dr. Ko trabajaba en el laboratorio de Pedersen. El Dr. Ko y Pedersen estudiaron juntos desde 1991.
Tal como lo diseñó especialmente el Dr. Ko, mientras que las células tumorales se destruyen rápidamente cuando se tratan con 3BP, las células normales no se ven afectadas.
Esto se debe a que los niveles de transportadores de ácido monocarboxílico (MCT) no aumentan en las células normales, a diferencia de las células tumorales.
Como explicaron el Dr. Ko y Pedersen, el MCT es un canal de transporte por donde el 3BP puede ingresar al interior de las células tumorales. Una vez dentro, 3BP destruye rápidamente toda la planta de energía de la célula tumoral (glucólisis y OxPhos).
Las células tumorales mueren rápidamente por muerte celular (apoptosis) o necrosis y la energía disminuye rápidamente.
3BP: Estructura y reacción química
La razón por la que 3BP tiene esta selectividad se debe a la similitud con las estructuras de ácido pirúvico y ácido láctico como se muestra a continuación.


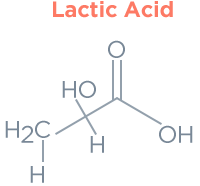
3BP transforma proteínas con (-SH, -NH2), bases de ácidos nucleicos y metabolitos. Como resultado de una reacción química en una célula cancerosa de este tipo, se interrumpe el metabolismo de la célula cancerosa.



Dos mecanismos de 3BP
El 3BP en las células cancerosas tiene dos mecanismos principales
Primero, bloqueo del metabolismo energético en las células cancerosas.
En segundo lugar, la recuperación de la función de apoptosis de las células cancerosas.
Primero, veamos un mecanismo que interfiere con el metabolismo energético de las células cancerosas.
Mecanismo 1: Cortando la línea de combustible de las células cancerosas
- En comparación con las células normales, las células cancerosas producen cantidades elevadas de ácido láctico en presencia de O2 (efecto Warburg)
- Los transportadores de ácido láctico (transportadores de monocarboxilato) están regulados positivamente en las células cancerosas.
- Debido a la similitud estructural con el ácido láctico, 3BP ingresa preferentemente a las células cancerosas
- Dentro de las células cancerosas, 3BP inhibe las dos plantas de energía (glucólisis y fosforilación oxidativa mitocondrial)
- Las reservas de energía celular (ATP) se agotan rápidamente
Hipótesis del caballo de Troya para la acción selectiva de 3BP en células cancerosas
(Se cuela por las puertas por las que sale lactato y destruye las "plantas de energía".)

Mecanismo 2: Recuperación funcional de VDAC (apoptosis)
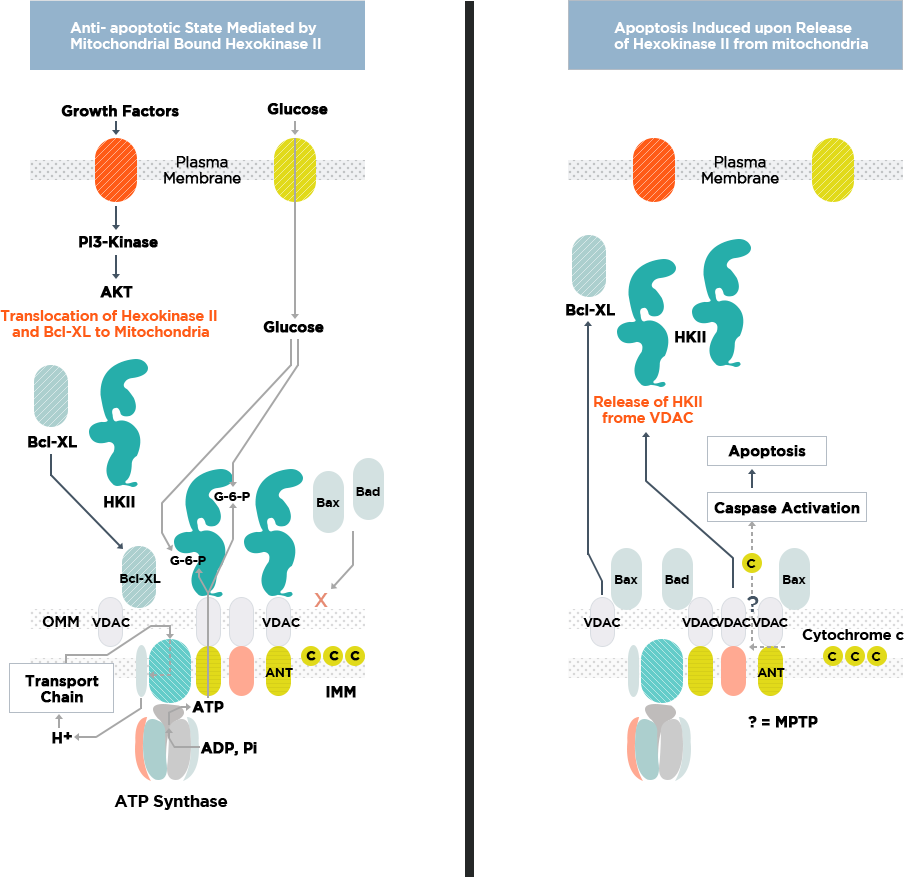
La hexoquinasa unida a mitocondrias (HK) II juega un papel importante en la prevención de la apoptosis tumoral.
Derecha: Sin los mecanismos de control establecidos para prevenirla, la muerte celular sería muy probable dentro de las condiciones desfavorables que existen en un microambiente tumoral. Así, la inducción de apoptosis mediada por caspasa se facilitaría primero mediante la activación del complejo de poros de transición de permeabilidad mitocondrial (MPTP), indicado a la derecha por un signo de interrogación (?), Que a su vez facilitaría la liberación al citoplasma de la caspasa. citocromo c activador (ubicado dentro del espacio entre membranas). Las proteínas relacionadas con Bcl-2 (Bax y Bad) probablemente superarían los efectos de la proteína inhibidora de MPTP Bcl-XL y ayudarían a facilitar la liberación del citocromo c.
Izquierda: al poblar los canales aniónicos dependientes de voltaje (VDAC) mitocondriales con HK II y mediante la canalización persistente de nucleótidos de adenina, se inhibe la apertura del MPTP. Esto, a su vez, inhibe el acceso de los VDAC a Bax y Bad, y muy probablemente mantiene el citocromo c en un estado favorable para su retención mitocondrial en el espacio entre membranas. Por lo tanto, HK II ayuda a asegurar la proliferación de un tumor altamente maligno y su escape de la muerte celular, en condiciones que de otro modo favorecerían este proceso.
Estrategias terapéuticas dirigidas al metabolismo
Los fármacos que interfieren con el metabolismo energético, como el 3BP, se están estudiando actualmente de varias formas.
En la siguiente figura, resumimos los medicamentos que funcionan en el transcurso de 1 a 6.
(1) Dirigirse a enzimas clave (hexoquinasa 2) en la glucólisis en etapa temprana> 3BP, DG (desoxiglucosa), lonidamina
(2) Inhibir ATP sintasoma (ATP sintasa / complejo portador de nucleótidos de adenina / portador de fosfato)> 3BP
(3) Eflujo de lactato objetivo> ácido alfa ciano 4-hidroxicinámico (ACCA)
(4) (5) Lactato deshidrogenasa diana (LDH), piruvato deshidrogenasa (PDH), piruvato deshidrogenasa quinasa (PDHK)
que relacionado con la entrada de piruvato mitocondrial> 3BP (Inhibir LDH), DCA (Inhibir dicloroacetato; PDHK)
(6) La piruvato quinasa objetivo> MITAPIVAT (Agios) activa la piruvato quinasa-R (PKR) que aparece en los glóbulos rojos para tratar la deficiencia de PK
(Fase 2/3, designación de medicamento huérfano y vía rápida)
Etc.: Reducir la transferencia tumoral al neutralizar el pH bajo en el microambiente tumoral> terapia con bicarbonato, terapia 3BP
3BP reduce el nivel de ATP por debajo del 20% al bloquear la generación de ATP en el metabolismo energético del cáncer simultáneamente en varios procesos.
En otras palabras, es matar las células cancerosas.

Resumen
Mecanismo 1:
Las células cancerosas operan canales para liberar un nivel de pH excesivo debido a la saturación del ácido lactato, ya que puede causar la muerte de las células cancerosas.
(MCT - Transportadores monocarboxilatos)
3BP (3Bromopiruvato, BrCH2COCO2H) es un fármaco que hace que las células cancerosas mueran de hambre a través de los siguientes mecanismos.
1) Ingrese selectivamente a las células cancerosas a través de MCT como ácido láctico (efecto caballo de Troya)
2) Combinando con Hexokinase2 para inhibir la reacción química (inhibidor)
3) Inhibición de LDH (lactato deshidrogenasa)
Entrar en la mitocondria a través del canal de piruvato como ácido piruvato
Inhibición del metabolismo mitocondrial (combinar con ATPasa para desactivar su función)
Mecanismo 2:
3BP surgen reacción química con HK2
Entonces HK2 no puede bloquear bcl-xl combinar con VDAC
Recuperación funcional de VDAC (habilita la apoptosis)
