Startpunt van KAT

Er zijn verschillende generaties therapieën die naast elkaar bestaan als middelen tegen kanker.
Maar toch is de verovering van kanker ver weg.Het grootste probleem van de huidige behandeling tegen kanker is toxiciteit.
Met andere woorden, omdat er geen selectiviteit is voor kankercellen.We ontwikkelen een antikankermiddel dat de vierde generatie antikankermiddelen wordt genoemd.
KAT verwijst naar de antikankerbehandelingstechnologie die is ontwikkeld door Dr. Ko KAT = Kodiscovery Anticancer TechnologyDeze techniek komt voort uit een klein molecuul genaamd 3-bromopyruvaat (3BP), ontdekt door Dr. Young Hee Ko toen Dr. Ko in het laboratorium van Pedersen werkte. Dr. Ko en Pedersen studeerden samen sinds 1991.
Zoals speciaal ontworpen door Dr. Ko, terwijl tumorcellen snel worden vernietigd wanneer ze worden behandeld met 3BP, worden normale cellen niet aangetast.
Dit komt doordat de monocarbonzuurtransporters (MCT's) -niveaus in normale cellen niet stijgen, in tegenstelling tot tumorcellen.
Zoals Dr. Ko en Pedersen hebben uitgelegd, is MCT een transportkanaal waar 3BP de binnenkant van tumorcellen kan binnendringen. Eenmaal binnen vernietigt 3BP snel de hele energiecentrale van de tumorcel (glycolyse en OxPhos).
Tumorcellen sterven snel af door celdood (apoptose) of necrose en de energie neemt snel af.
3BP: Structuur en chemische reactie
De reden dat 3BP deze selectiviteit heeft, is te wijten aan de gelijkenis met de structuren van pyrodruivenzuur en melkzuur, zoals hieronder weergegeven.


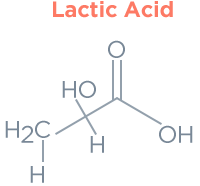
3BP transformeert eiwitten met (-SH, -NH2), nucleïnezuurbasen en metabolieten. Door een chemische reactie in zo'n kankercel wordt het metabolisme van de kankercel verstoord.



Twee mechanismen van 3BP
De 3BP in de kankercellen heeft twee belangrijke mechanismen
Ten eerste, blokkering van het energiemetabolisme in kankercellen.
Ten tweede, het herstel van de apoptosefunctie van kankercellen.
Laten we eerst eens kijken naar een mechanisme dat het energiemetabolisme van kankercellen verstoort.
Mechanisme 1: Doorsnijden van de brandstofleiding van de kankercellen
- In vergelijking met normale cellen produceren kankercellen verhoogde hoeveelheden melkzuur in aanwezigheid van O2 (Warburg-effect)
- Melkzuurtransporters (monocarboxylaattransporters) worden opwaarts gereguleerd in kankercellen
- Vanwege structurele gelijkenis met melkzuur komt 3BP bij voorkeur kankercellen binnen
- In kankercellen remt 3BP de twee energiecentrales (glycolyse en mitochondriale oxidatieve fosforylatie)
- De cellulaire energie (ATP) reserves raken snel uitgeput
Hypothese van Trojaans paard voor selectieve actie van 3BP op kankercellen
(Sluipt naar binnen door deuren waar lactaat naar buiten gaat en vernietigt "energiecentrales".)

Mechanisme 2: Functioneel herstel van VDAC (apoptose)
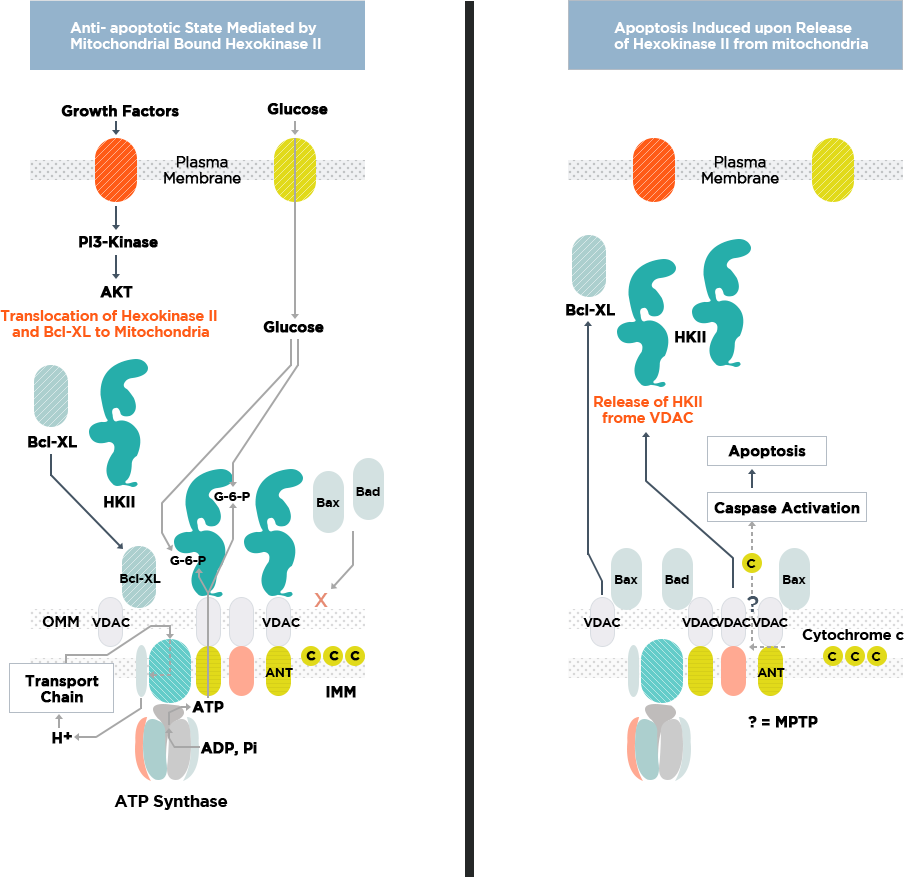
Mitochondriaal gebonden hexokinase (HK) II speelt een belangrijke rol bij het voorkomen van tumorapoptose.
Rechts: zonder controlemechanismen om het te voorkomen, zou celdood zeer waarschijnlijk zijn binnen de ongunstige omstandigheden die bestaan in een tumor micro-omgeving. Caspase-gemedieerde inductie van apoptose zou dus eerst worden vergemakkelijkt door activering van het mitochondriale permeabiliteitstransitieporiëncomplex (MPTP), rechts aangegeven met een vraagteken (?), Dat op zijn beurt de afgifte van de caspase aan het cytoplasma zou vergemakkelijken. activator cytochroom c (gelegen in de intermembraanruimte). Bcl-2-gerelateerde eiwitten (Bax en Bad) zouden waarschijnlijk de effecten van het MPTP-remmende eiwit Bcl-XL overwinnen en de afgifte van cytochroom c vergemakkelijken.
Links: Door mitochondriale spanningsafhankelijke anionkanalen (VDAC's) te vullen met HK II en door aanhoudende kanalisatie van adeninenucleotiden, wordt het openen van het MPTP geremd. Dit remt op zijn beurt de toegang van VDAC's tot Bax en Bad, en houdt hoogstwaarschijnlijk cytochroom c in een toestand die gunstig is voor zijn mitochondriale retentie in de intermembraanruimte. HK II helpt dus bij het verzekeren van de proliferatie van een zeer kwaadaardige tumor en het ontsnappen aan celdood, onder omstandigheden die dit proces anders zouden begunstigen.
Metabole gerichte therapeutische strategieën
Geneesmiddelen die het energiemetabolisme verstoren, zoals 3BP, worden momenteel op een aantal manieren bestudeerd.
In de onderstaande figuur hebben we de medicijnen samengevat die in de loop van 1 op 6 werken.
(1) Gericht op sleutelenzymen (hexokinase 2) in de vroege fase van glycolyse > 3BP, DG (deoxyglucose), lonidamine
(2) Remmen van ATP-synthasoom (ATP-synthase / adenine-nucleotidedrager / fosfaatdragercomplex) > 3BP
(3) Doellactaatefflux > alfa-cyano-4-hydroxykaneelzuur (ACCA)
(4) (5) Target lactaat dehydrogenase (LDH), pyruvaat dehydrogenase (PDH), pyruvaat dehydrogenase kinase (PDHK)
wat verband hield met de toegang tot mitochondriaal pyruvaat > 3BP (remt LDH), DCA (remt dichlooracetaat; PDHK)
(6) Doelpyruvaatkinase > MITAPIVAT (Agios) activeert pyruvaatkinase-R (PKR) dat in rode bloedcellen verschijnt om PK-deficiëntie te behandelen
(Fase 2/3, Weesgeneesmiddel en Fast Track-status)
Enz.: Verminder de tumoroverdracht door de lage pH in de micro-omgeving van de tumor te neutraliseren > bicarbonaattherapie, 3BP-therapie
3BP verlaagt het ATP-niveau onder de 20% door de vorming van ATP in het energiemetabolisme van kanker gelijktijdig in verschillende processen te blokkeren.
Met andere woorden, het is om de kankercellen te doden.

Overzicht
Mechanisme 1:
Kankercellen gebruiken kanalen om een te hoog pH-niveau vrij te maken als gevolg van lactaatzuurverzadiging, omdat dit de dood van kankercellen kan veroorzaken.
(MCT's - monocarboxylaat transporters)
3BP (3Bromopyruvate, BrCH2COCO2H) is een medicijn dat ervoor zorgt dat kankercellen van honger afsterven via de volgende mechanismen.
1) Selectief kankercellen binnenkomen via MCT als melkzuur (Trojan Horse Effect)
2) Combinatie met Hexokinase2 om chemische reactie te remmen (remmer)
3) Remming van LDH (lactaatdehydrogenase)
Ga mitochondriën binnen via het pyruvaatkanaal als pyruvaatzuur
Remming van mitochondriaal metabolisme (combineer met ATPase om zijn functie te deactiveren)
Mechanisme 2:
3BP ontstaat een chemische reactie met HK2
HK2 kan dus de combinatie van bcl-xl met VDAC niet blokkeren
VDAC's functioneel herstel (apoptose inschakelen)
