Punkt startu KAT

Istnieje kilka generacji terapii, które opierają się na lekach przeciwnowotworowych.
Jednak droga do pokonania raka jest daleka.Największym obecnie problemem leczenia nowotworów jest toksyczność leków.
Inaczej mówiąc nie ma specyficzności leków tylko dla komórek rakowych.Aktualnie opracowujemy środek przeciwnowotworowy określony jako czwarta generacja leków przeciwnowotworowych.
KAT odnosi się do technologii leczenia przeciwnowotworowego, którą opracowała dr Ko KAT = Kodiscovery Anticancer TechnologyTechnika ta dotyczy małej cząsteczki zwanej 3-bromopirogronianem (3BP), odkrytej przez dr Young Hee Ko, podczas pracy badawczej w laboratorium Pedersena. Dr Ko i Pedersen prowadzili razem badania od 1991 roku.
Procedura specjalnie opracowana przez dr Ko powoduje szybkie niszczenie komórek nowotworowych po potraktowaniu 3BP. Natomiast normalne komórki nie ulegają zmianie.
Dzieje się tak dlatego, że poziomy transporterów kwasu monokarboksylowego (MCT) nie rosną w normalnych komórkach, w przeciwieństwie do komórek nowotworowych.
Dr Ko i Pedersen wyjaśnili, że MCT jest kanałem transportowym przez który 3BP może dostać się do wnętrza komórek nowotworowych. Wewnątrz komórek 3BP szybko niszczy całą elektrownię komórek nowotworowych (glikolizę i OxPhos).
Komórki nowotworowe są szybko niszczone w wyniku śmierci komórki (apoptozy) lub martwicy (nekrozy), a poziom energii (ATP) gwałtownie spada.
3BP: Struktura i reakcja chemiczna
Powodem, dla którego 3BP ma tę selektywność, jest podobieństwo do struktur kwasu pirogronowego i kwasu mlekowego, jak pokazano poniżej.


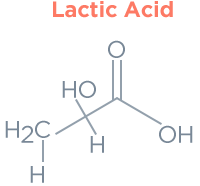
3BP przekształca białka za pomocą (-SH, -NH2), zasad kwasu nukleinowego i metabolitów. W wyniku reakcji chemicznej w takiej komórce rakowej metabolizm komórki zostaje zaburzony.



Dwa mechanizmy działania 3BP
3BP w komórkach nowotworowych wykazuje dwa główne mechanizmy działania
Po pierwsze, blokada metabolizmu energetycznego w komórkach nowotworowych.
Po drugie, przywrócenie funkcji apoptozy komórek rakowych.
Przede wszystkim przyjrzyjmy się mechanizmowi, który zakłóca metabolizm energetyczny komórek rakowych.
Mechanizm 1: Przecięcie linii dostarczającej paliwo komórkom rakowym.
- W porównaniu do normalnych komórek, komórki rakowe wytwarzają podwyższone ilości kwasu mlekowego w obecności O2 (efekt Warburga)
- Transportery kwasu mlekowego (transportery monokarboksylanów) są "regulowane w górę" (silniejsza ekspresja) w komórkach rakowych.
- Ze względu na strukturalne podobieństwo do kwasu mlekowego 3BP preferencyjnie przedostaje się do komórek rakowych
- Wewnątrz komórek nowotworowych 3BP hamuje dwie elektrownie (glikolizę i mitochondrialną fosforylację oksydacyjną)
- Rezerwy energii komórkowej (ATP) szybko się wyczerpują
Hipoteza konia trojańskiego oparta na specyficznym działaniu 3BP na komórki rakowe.
(Zakrada się przez drzwi, przez które wychodzi mleczan i niszczy „elektrownie”).

Mechanizm 2: Przywrócenie funkcji VDAC (apoptoza).
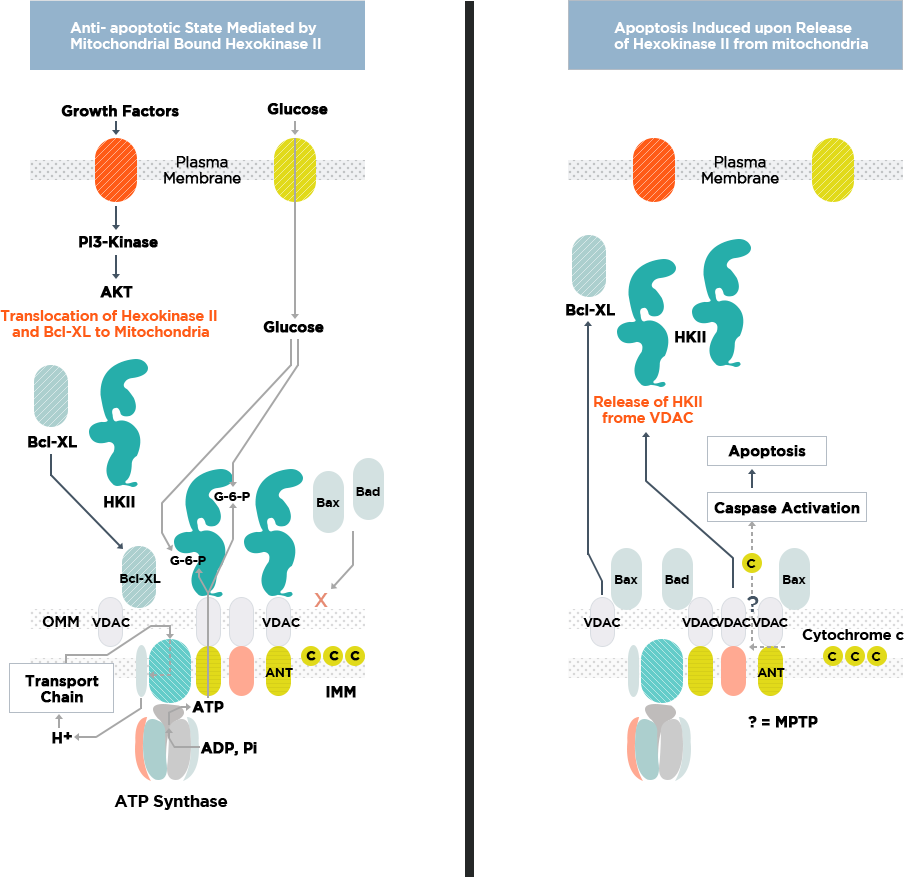
Heksokinaza związana z mitochondriami (HK) II odgrywa główną rolę w zapobieganiu apoptozy guza.
Po prawej: bez obecności mechanizmów kontrolnych zapobiegających, śmierć komórki byłaby wysoce prawdopodobna w niekorzystnych warunkach, które istnieją w mikro środowisku guza. Tak więc indukcja apoptozy za pośrednictwem kaspazy byłaby ułatwiona przede wszystkim przez aktywację przejścia kompleksu mitochondrialnego dzięki przepuszczalności porów (MPTP), oznaczonego po prawej stronie znakiem zapytania (?), To z kolei ułatwiłoby uwolnienie kaspazy do cytoplazmy. Aktywator cytochromu c jest zlokalizowany w przestrzeni międzybłonowej. Białka związane z Bcl-2 (Bax i Bad) prawdopodobnie przezwyciężają wpływ białka hamującego MPTP Bcl-XL i ułatwiają uwalnianie cytochromu c.
Po lewej: poprzez wypełnienie mitochondrialnych kanałów anionowych zależnych od napięcia (VDAC) HK II i trwałe "kanałowanie" nukleotydów adeninowych, otwarcie MPTP jest hamowane. To z kolei hamuje dostęp VDAC do Bax oraz Bad i najprawdopodobniej utrzymuje cytochrom c w stanie sprzyjającym jego retencji mitochondrialnej w przestrzeni międzybłonowej. Tak więc HK II zapewnia proliferację wysoce złośliwego guza i jego ucieczkę przed śmiercią komórkową w warunkach, które w innym przypadku sprzyjałyby temu procesowi.
Strategie terapeutyczne ukierunkowane na metabolizm komórkowy.
Leki, które zakłócają metabolizm energetyczny, takie jak 3BP są obecnie badane na kilka sposobów.
Na poniższym rysunku podsumowaliśmy leki, które działają na etapach od 1 do 6.
(1) Celowanie w kluczowe enzymy (heksokinaza 2) we wczesnym etapie glikolizy > 3BP, DG (deoksyglukoza), Lonidamina
(2) Hamowanie syntasomu ATP (syntaza ATP / kompleks nośnika nukleotydów adeninowych / kompleks nośników fosforanowych) > 3BP
(3) Docelowy wypływ mleczanu > kwas alfa cyjano-4-hydroksycynamonowy (ACCA)
(4) (5) Docelowa dehydrogenaza mleczanowa (LDH), dehydrogenaza pirogronianowa (PDH), kinaza dehydrogenazy pirogronianowej (PDHK)
co związane z wejściem pirogronianu do mitochondriów > 3BP (hamowanie LDH), DCA (hamowanie dichlorooctanu;PDHK)
(6) Docelowa kinaza pirogronianowa > MITAPIVAT (Agios) aktywuje kinazę pirogronianową-R (PKR), która pojawia się w czerwonych krwinkach w celu leczenia niedoboru PK
(Faza 2/3, lek sierocy i oznaczenie w trybie Fast Track)
Itp.: Ograniczenie przenoszenia guza poprzez neutralizację niskiego pH w mikrośrodowisku guza > terapia wodorowęglanowa, terapia 3BP
3BP obniża poziom ATP poniżej 20% blokując wytwarzanie ATP w metabolizmie energetycznym komórek raka jednocześnie w różnych procesach.
Inaczej mówiąc, chodzi o zabicie komórek rakowych.

Podsumowanie
Mechanizm 1:
Komórki rakowe obsługują kanały uwalniające nadmierny poziom pH z powodu nasycenia kwasem mlekowym, ponieważ może to spowodować śmierć komórek rakowych.
(MCT - transportery monokarboksylanów)
3BP (3Bromopyruvate, BrCH2COCO2H) to lek, który powoduje śmierć komórek rakowych z głodu w wyniku następujących mechanizmów.
1) Selektywnie dostaje się do komórek rakowych poprzez MCT naśladując kwas mlekowy (efekt konia trojańskiego).
2) Łączenie z Hexokinazą 2 w celu zahamowania reakcji chemicznej (Inhibitor).
3) Hamowanie LDH (dehydrogenaza mleczanowa).
4) Wnika do mitochondriów kanałem pirogronianowym jako kwas pirogronowy.
5) Hamuje metabolizm mitochondriów (w połączeniu z ATPazą w celu dezaktywacji jej funkcji)
Mechanizm 2:
3BP generuje reakcję chemiczną z HK2.
W konsekwencji HK2 nie może blokować łączenia bcl-xl z VDAC.
Przywrócenie funkcjonalnego VDAC (umożliwia apoptozę).
